Correio Braziliense
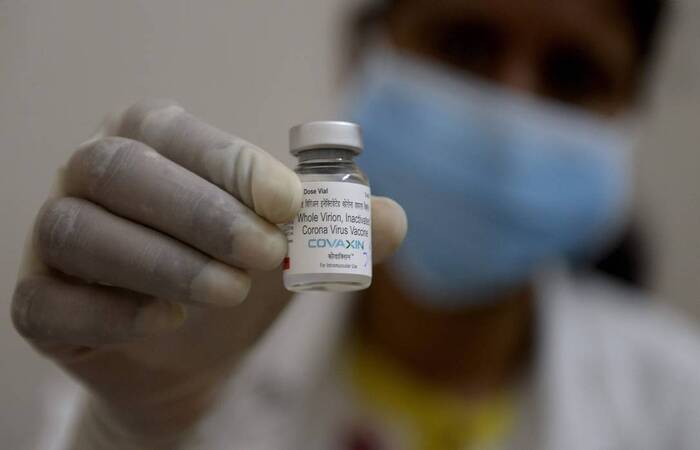
A diretoria colegiada da Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, na noite de ontem (4), a importação das vacinas Covaxin, da Índia, e da Sputinik V, da Rússia. Quatro diretores, de cinco, votaram a favor da importação excepcional e temporária dos imunizantes para fins de distribuição e uso no Brasil.
Os países produtores terão que atender as condições estabelecidas pela área técnica do órgão. As duas vacinas devem ser utilizadas apenas entre adultos de 18 a 60 anos, fornecer bulas em português, terem os lotes importados aprovados por laboratórios certificados. Além disso, é preciso implantar um programa de monitoramento de eventos adversos.
“Destaco que fica autorizada a importação excepcional e temporária do seguinte quantitativo, correspondente a doses para imunização de 1% da população nacional, dentro do cronograma enviado pelo Ministério da Saúde: 4 milhões de doses”, disse Alex Machado Campos, diretor da agência.
Com a aprovação dos imunizantes, o governo federal espera receber ao menos 20 milhões de doses da vacina indiana. Já havia acordo para a aquisição com o laboratório responsável. As doses da Sputnik V, solicitadas pelos governos da Bahia, Maranhão, Sergipe, Ceará, Pernambuco e Piauí, também poderão ser utilizadas no país. No entanto, a decisão exige a aquisição de uma quantidade menor de vacinas, para que a qualidade do produto seja testada.
O gerente-geral de Medicamentos e Produtos Biológicos, Gustavo Mendes Lima Santos, ressaltou, em seu parecer, que a área técnica da Anvisa não está atestando a qualidade, a segurança e a eficácia dos dois imunizantes, mas apresentando seu parecer conforme determina uma lei sobre a importação emergencial de vacinas por ocasião da pandemia. Ainda há necessidade de aprovação pelo Instituto Nacional de Controle de Qualidade em Saúde (INCQS).
Pedido negado
Esta é a segunda vez que a Anvisa analisa o pedido de importação e uso desses imunizantes. Na primeira avaliação da Covaxin, em março deste ano, o órgão recusou a solicitação feita pelo Ministério da Saúde por não identificar nos dados apresentados pela Índia os requisitos de lei para atestar a qualidade do produto. Em abril, a Sputnik V foi rejeitada por falta de dados.